酰胺结构单元广泛存在于蛋白质及药物、精细化学品中。5-氰基戊酰胺(5-CVAM)作为己二腈(ADN)水合的单酰胺产物,是合成除草剂唑啶草酮的关键前体,具有重要工业价值。腈水合酶(NHase)催化路线因绿色、温和、高效,被认为是5-CVAM合成的理想替代工艺。
大连理工大学化工海洋与生命学院梁长海教授团队前期发现并改造了一种对脂肪族二腈具有显著底物选择性的腈水合酶(ReNHase),并通过优化RBS序列促进了该酶α/β亚基的平衡表达,使酶的比活力提高近12倍(ChemBioChem 2024, 25, e202400526;中国专利ZL 202310433598.2)。但发现催化效率大幅提升导致对5-CVAM的区域选择性下降,造成副产物己二酰胺(ADM)的累积。
为解决该问题,梁长海教授团队采用半理性设计策略,预测并筛选了位于底物通道与结合口袋的关键残基,剔除高度保守及活性相关位点后构建突变体文库。经酶动力学表征,锁定调控ADN水合区域选择性的关键位点βTyr72,获得对5-CVAM区域选择性分别达96%和100%的突变体βY72A与βY72C。
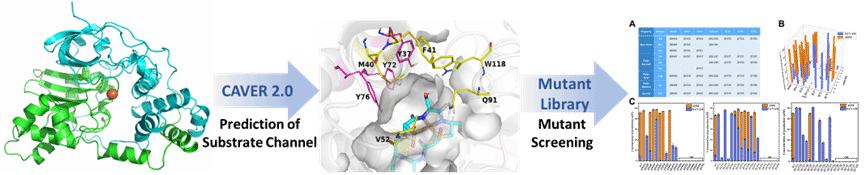
通过底物通道构象、结合口袋体积、分子对接及分子动力学模拟,解析了两种突变体提升区域选择性的结构基础。揭示了βTyr72作为“开关”残基,在调控ADN水合反应的区域选择性与催化活性方面发挥关键结构作用。
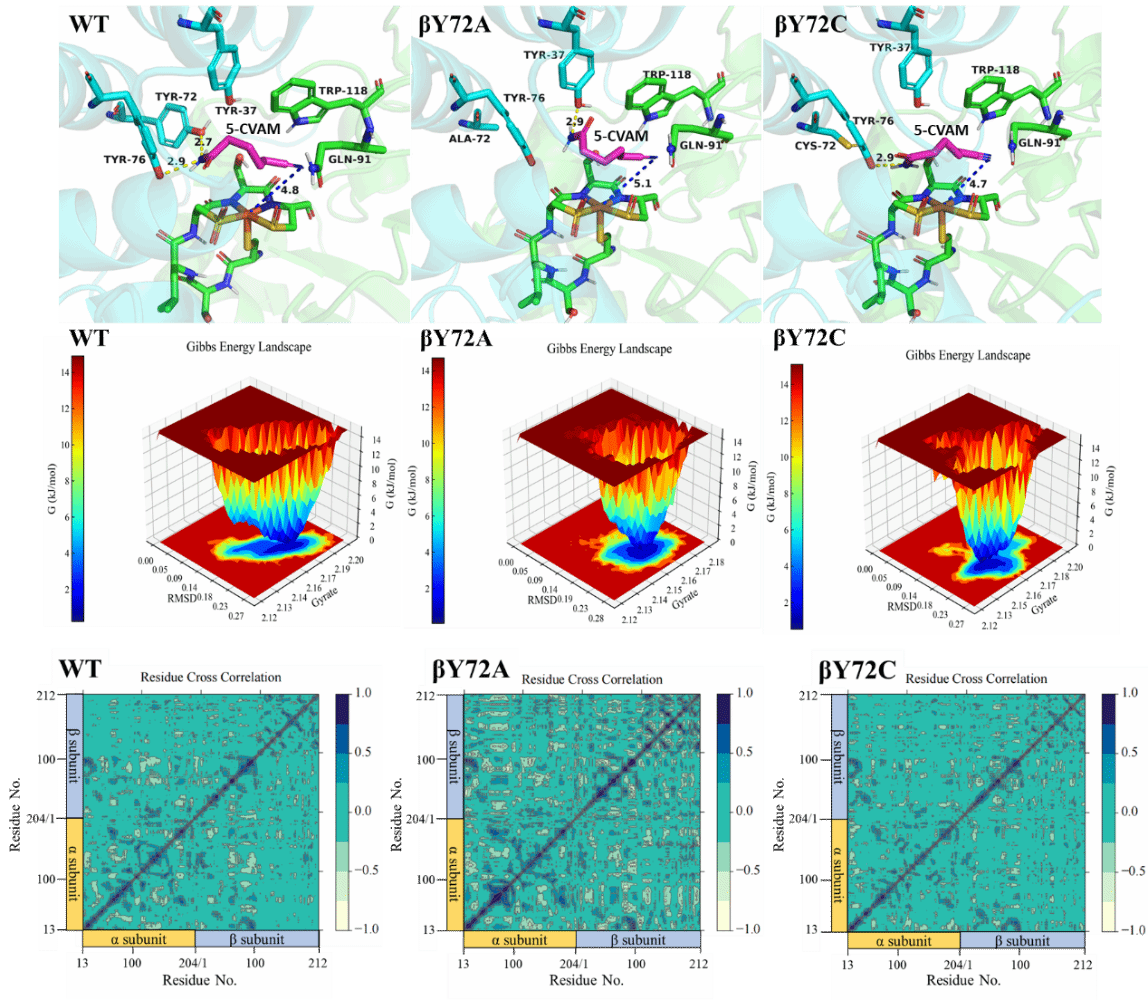
相关成果以“Reprogramming Regioselectivity of Nitrile Hydratase towards Adiponitrile via Semi-rational Design of a Key ‘Switch’ Residue”为题发表于International Journal of Biological Macromolecules(2026, 357, 151582)。该期刊为生物学领域知名TOP期刊(IF=8.7)。论文第一作者为博士生郭祎,通讯作者为梁长海教授与王黎副教授。相关技术已获中国发明专利授权(ZL 2024 1 1198452.5)。基于该突变菌株的5-CVAM生物制造放大验证工作正在大连理工大学成都研究院推进,取得重要进展。
文章链接:https://doi.org/10.1016/j.ijbiomac.2026.151582。